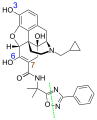納地美定
 | |
| 臨床資料 | |
|---|---|
| 商品名 | Symproic, Rizmoic |
| 其他名稱 | S-297,995 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a617031 |
| 核准狀況 | |
| 給藥途徑 | 口服 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 血漿蛋白結合率 | 93–94% |
| 藥物代謝 | 主要經由 CYP3A4 |
| 生物半衰期 | 11 hrs |
| 排泄途徑 | 尿液、糞便 |
| 識別資訊 | |
| |
| CAS號 | 916072-89-4 1345728-04-2(對甲苯磺酸鹽) |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| 化學資訊 | |
| 化學式 | C32H34N4O6 |
| 摩爾質量 | 570.65 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
納地美定 (台灣商品名適秘效,美國商品名Symproic ,歐盟地區商品名Rizmoic ),是一種口服末梢性µ型類鴉片受體拮抗劑,用於治療成年人患有非因癌症所導致之慢性疼痛,因長期使用鴉片類藥物所致之便秘。本藥物由鹽野義製藥開發,[1]臨床研究發現它對上述適應症的效果具有統計學上的意義,一般來說病人耐受度良好,副作用主要為輕至中度的腸胃道副作用, [2]僅有少數病人發生中樞神經系統鴉片類藥物戒斷症狀,或是影響了同時給予的鴉片類藥物的止痛或縮瞳效果。 [3]
醫療用途
[編輯]美國核准納地美定治療患有慢性非癌症疼痛的成人,因使用鴉片類藥物所導致的便秘,包括因先前的癌症或其治療相關的慢性疼痛,且不需要頻繁增加鴉片類止痛藥物劑量的病人。 [3]
在歐盟,納地美定也被核准治療成年人因鴉片類藥物導致的便秘,作為瀉劑治療後的二線用藥。 [4]
禁忌症
[編輯]禁用於腸胃道阻塞或穿孔病人,或有這些問題風險的患者。 [3] [4]
副作用
[編輯]研究時發現的副作用如下:腹痛(用藥組發生率8-11%,安慰劑組為 2-5%)、腹瀉(7%,安慰劑組2-3%)、噁心(4-6%,安慰劑組2- 5%)、嘔吐(3%,安慰劑組2%)、腸胃炎(2-3%,安慰劑組1%),以及鴉片類藥物戒斷症候群(1.5-3.2% ,對安慰劑組為0.5-1.5%)。後者除一位病人發生嚴重但可處理的副作用外,皆為輕至中度。超敏反應少見,僅有兩位病人。 [3] [4]
過量
[編輯]單次給予高達建議劑量的500倍劑量,以及給予高達推薦劑量的150倍之劑量持續10天,會導致前述副作用增加,但僅為輕度到中度之嚴重程度。 [3] [4]
交互作用
[編輯]納地美定主要由肝臟的酵素CYP3A4代謝,故此酵素的抑制劑將增加納地美定的體內濃度,可能增加其副作用。例如伊曲康唑(增加了納地美定的暴露量達2.9倍)、酮康唑、克拉黴素和葡萄柚汁。相對地,CYP3A4的誘導劑如利福平和聖約翰草將降低納地美定在體內的濃度;利福平可降低納地美定濃度達 83%。 [3] [4]
P-糖蛋白的強抑制劑(如環孢素)可能會增加血漿中的納地美定濃度。 [3] [4]
藥理
[編輯]作用機轉
[編輯]納地美定是納曲酮的衍生物,並且可阻斷μ、δ和κ型鴉片受體。納地美定因能穿越血腦屏障而可用於治療鴉片類藥物依賴性。但納地美定因為有巨大的親水性側鏈,以及與P-醣蛋白的親和力,故納地美定在中樞神經系統中的濃度極低,反而主要作用於腸胃道的μ型鴉片受體,對抗鴉片類藥物導致的便秘。 [4]
藥代動力學
[編輯]口服後,納地美定的絕對生物利用度介於20%至56%,空腹服用0.75小時後(與高量脂肪餐點一起服用 2.5 小時後)達到最高血漿濃度。與實務憶起服用或空腹服用,其藥物濃度曲線下面積沒有顯着差異,因此服藥時間與是否空腹無關。本藥物進入血液後,93%至94%的與血漿蛋白結合,主要是白蛋白。 [3] [4]
納地美定主要由CYP3A4代謝為去甲基納地美定[5](約占循環中本物質的9-13%),部分由UGT1A3代謝為納地美定3-葡糖苷酸,次要代謝物物包括 6-葡糖苷酸、7-( R/S )-羥基衍生物,以及腸細菌裂解噁二唑環形成納地美定羧酸與苯甲脒。去甲基納地美定與含葡糖苷酸根和羧酸根的衍生物,也可以拮抗鴉片類受體,但不如原始藥物有效。 [6]
-
去甲基納地美定,主要代謝物
納地美定及其代謝物經由尿液和糞便排泄。終末半衰期約為11小時。 [4] [6]
化學
[編輯]納地美定藥物為甲苯磺酸鹽的形式,呈白至淺褐色粉末狀,不吸濕,在生理pH值下具有高水溶性。 [6]
社會與文化
[編輯]臨床試驗
[編輯]COMPOSE計劃是在18-80歲患有慢性非癌症疼痛,但因使用鴉片類藥物導致便秘的成年人,所進行的三期臨床試驗。COMPOSE-I和COMPOSE-II是為12周的隨機雙盲對照試驗,比較納地美定與安慰劑的效果。COMPOSE-I於2013年8月至2015年1月在七個國家的68家門診單位進行,而COMPOSE-II於2013年11月開始至2015年6月在六個國家的69個門診單位進行。在這兩項試驗中,病人被隨機分配接受納地美定0.2毫克或安慰劑,每天一次,持續12周。治療有反應的定義為每周至少有3次自發排便,且在12周試驗期間的9周中有增加1次自發排便,包括研究最後4周中的3周。在COMPOSE-I和COMPOSE-II中,納地美定組的反應者比例顯着高於安慰劑組。兩項試驗中的不良事件相似,然而使用納地美定組患者的不良事件發生率略高。 [7]
COMPOSE-III是為期52周的臨床試驗,旨在研究納地美定在非癌症慢性疼痛患者中的長期安全性。結果發現在統計學上病人每周排便增加,且並未有鴉片類藥物戒斷症狀,結論為兩組之間的不良反應相似。 [8]
參考
[編輯]- ^ FDA Approves Symproic (naldemedine) for the Treatment of Opioid-Induced Constipation - Chemdiv. Chemdiv. 2017-03-27 [2017-04-05]. (原始內容存檔於2017-04-06) (美國英語).
- ^ Shionogi. Research and Development at Shionogi (as of March 2009) (PDF). 2009-03-27 [2012-05-12]. (原始內容 (PDF)存檔於2013-05-22).
- ^ 3.0 3.1 3.2 3.3 3.4 3.5 3.6 3.7 FDA專業藥物信息 on Symproic.
- ^ 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 4.8 Rizmoic: EPAR – Product information (PDF). European Medicines Agency (EMA). 2019-08-29 [2022-08-25]. (原始內容存檔 (PDF)於2021-10-28).
- ^ Ohnishi S, Fukumura K, Kubota R, Wajima T. Absorption, distribution, metabolism, and excretion of radiolabeled naldemedine in healthy subjects. Xenobiotica; the Fate of Foreign Compounds in Biological Systems. September 2019, 49 (9): 1044–1053. PMID 30351180. S2CID 53036507. doi:10.1080/00498254.2018.1536815.
- ^ 6.0 6.1 6.2 Rizmoic: EPAR – Public assessment report (PDF). European Medicines Agency (EMA). 2018-12-14 [2022-08-25]. (原始內容存檔 (PDF)於2021-10-28).
- ^ Hale M, Wild J, Reddy J, Yamada T, Arjona Ferreira JC. Naldemedine versus placebo for opioid-induced constipation (COMPOSE-1 and COMPOSE-2): two multicentre, phase 3, double-blind, randomised, parallel-group trials. The Lancet. Gastroenterology & Hepatology. August 2017, 2 (8): 555–564. PMID 28576452. doi:10.1016/S2468-1253(17)30105-X.
- ^ Center for Drug Evaluaiton and Research Medication Review (PDF). FDA. FDA. [31 October 2017]. (原始內容存檔 (PDF)於2019-07-02).