J·J·湯木生
此條目需要補充更多來源。 (2015年5月15日) |
| J·J·湯木生 Joseph John Thomson 爵士 | |
|---|---|
 | |
| 出生 | 1856年12月18日 |
| 逝世 | 1940年8月30日(83歲) |
| 國籍 | |
| 母校 | 曼徹斯特維多利亞大學 劍橋大學 |
| 知名於 | 葡萄乾布丁模型 電子 同位素 質譜 電磁波導 湯木生散射 |
| 獎項 | 科普利獎章(1914年) |
| 科學生涯 | |
| 研究領域 | 物理學家 |
| 機構 | 劍橋大學 普林斯頓大學 耶魯大學 |
| 博士導師 | 約翰·斯特拉特 愛德華·勞思 |
| 博士生 | 查爾斯·威耳遜 歐尼斯特·拉塞福 約翰·西利·湯森德 歐文·理查森 威廉·亨利·布拉格 愛德華·阿普爾頓 |
| 其他著名學生 | 查爾斯·巴克拉 其子喬治·湯木生 弗朗西斯·阿斯頓 羅伯特·歐本海默 馬克斯·玻恩 保羅·朗之萬 傑弗里·泰勒 尼爾斯·波耳 |
| 簽名 | |
 | |
約瑟夫·約翰·湯木生爵士[註 1] OM FRS(Sir Joseph John "J. J." Thomson,1856年12月18日—1940年8月30日)[1],英國物理學家,諾貝爾物理學獎獲得主, 他發現了電子並測定了其質荷比,這是第一個被發現的次原子粒子。
1897年,湯木生表明,陰極射線由以前未知的帶負電粒子(現稱為電子)組成,他計算出這種粒子必須比原子小得多,並且有非常小的質荷比[2]。 湯木生在1913年也發現了穩定(非放射性)元素同位素的第一個證據,這是他在探索陽極射線(正離子)的過程中的成果之一。 他與弗朗西斯·阿斯頓一起確定帶正電粒子的性質的實驗是質譜法的第一次使用,使得質譜儀的發展[2]。
湯木生因其在氣體導電方面的工作而被授予1906年諾貝爾物理學獎[3]。
教育和個人生活
[編輯]湯木生1856年出生於英格蘭的曼徹斯特附近,蘇格蘭人家庭。1870年,他在不尋常年輕的14歲就被錄取在曼徹斯特的歐文學院(現在的曼徹斯特維多利亞大學)學習了工程學,搬到了劍橋大學三一學院。1884年12月22日,他被任命成為劍橋大學卡文迪許物理學教授[2],即卡文迪許實驗室主任[4]。他的學生之一是歐尼斯特·拉塞福,拉塞福於1919年接替湯木生就任卡文迪許物理學教授。 受到詹姆斯·馬克士威工作的影響和X射線的發現,他推導出陰極射線(參見陰極射線管)存在於帶負電的粒子,他稱之為「微粒」,這種微粒現在認識為電子。電子曾經被約翰斯東·斯通尼提出過,作為電化學中電荷的單位,但是湯木生認識到電子也是次原子粒子,這一點是第一次被發現。1897年他的發現為人所知,並在科學圈內引起了轟動,並最終於1906年被授予諾貝爾物理學獎[3]。
家庭
[編輯]1890年,湯木生娶了羅絲·佩傑特(Rose Elisabeth Paget),他的前學生之一[5] 。她是喬治·愛德華·佩傑特爵士的女兒(喬治·愛德華·佩傑特,英國劍橋醫學教授兼醫師。)他們育有一子喬治與一女瓊(Joan Paget Thomson)。極富戲劇性的是,他的兒子喬治·湯木生後來因證實電子是一種波而被授予諾貝爾物理學獎。(參見波粒二象性)
成就
[編輯]發現電子
[編輯]在湯木生以前,威廉·普朗特、諾曼·洛克耶等數名科學家就曾提出原子應該是由更基本的單元所組成,他們假設這個基本單元應與最輕的原子,氫原子有相同的大小。湯木生在1897年首先提出小於原子1000倍的次原子粒子,也就是現在所稱的電子。這項發現源自於湯木生對陰極射線性質的研究。在湯木生發現陰極射線(在當時被稱為萊納德射線)在空氣中行走的距離較於原子大小的粒子的所做預測還要更遠之後,1897年4月30日,他藉由測量陰極射線碰撞產生的熱與陰極射線的磁偏轉,估算出陰極射線的質量。實驗結果顯示陰極射線較氫原子輕1000倍,而且不論何種原子產生的陰極射線都有一樣的質量。湯木生判斷陰極射線是由非常輕且帶負電的粒子組成,而且是構成原子的普遍材料。他當時稱這粒子為「corpuscles」,然而而後的學界多使用「electron」稱呼電子,這個詞由喬治·斯托尼於1891年提出,早於湯木生實際發現電子。
在1897年4月,湯木生僅初步懷疑陰極射線可受電場偏轉(以往的研究者如海因里希·赫茲以為它們不會偏轉)。在湯木生提出了電子的一個月後,他發現將如果將陰極射線的放電管抽到非常低壓的狀態時,可以更有效的使陰極射線偏轉。藉由電場與磁場的偏轉,湯木生得以計算出電子的質荷比,並證實他之前的估計。這也成為測定電子質荷比的著名方法。(電子電荷的測量要到1909年羅伯特·密立坎油滴實驗。)
湯木生認為電子是從陰極射線管中的微量氣體發射出來的,他從而斷定原子是可分割的,電子就是原子的組成成分之一。1904年,湯木生提出梅子布丁模型,假設原子是帶正電的球體物質與其中的電子組成,為了解釋原子的電中性性質,電子分布在均勻的正電海中。
同位素與質譜法
[編輯]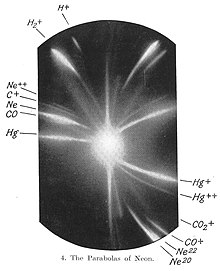
1912年,在湯木生研究陽極射線的過程中,他和他的研究助理弗朗西斯·阿斯頓引導氖離子流經過磁場和電場,並且藉著在路徑上放置感光板測量離子流的偏轉程度。他們觀察到感光板上有兩條曝光(如右圖),這說明氖離子流是由兩個不同的原子量的原子(分別是氖-20和氖-22)所組成的,也就是說此兩種不同的原子為同位素。弗雷德里克·索迪曾提出過同位素的存在可以解釋某些放射性物質的衰變,以上實驗首次證實穩定元素亦存在同位素。
約瑟夫.湯木生透過質量分離氖離子流而發現氖同位素是質譜法的第一個實例,隨後這個方法經由阿斯頓和登普斯特一同改善並且發展成普遍的方法[4]。
其他
[編輯]在1906年,湯木生證明了每一個氫原子只有一個電子。以前的理論中允許氫原子有不同數量的電子[7][8]。
陰極射線實驗
[編輯]磁偏轉
[編輯]湯木生首先研究有關陰極射線的磁偏轉。陰極射線是產生於裝置左邊的側管,並且藉由磁鐵的偏轉使陰極射線由陽極傳遞裝置的主鐘罩。湯木生透過檢測裝置中方形屏幕上的螢光路徑,他發現無論是在陽極或是在裝置內的氣體材料,光線的偏轉都會是相同的,而這也說明了陰極射線無論它的來源為何它都是相同的形式。
實驗證明陰極射線是帶電的
[編輯]陰極射線是否帶電在早期造成了兩大學派的爭論,分別是認為陰極射線是電磁波的乙太說以及認為陰極射線是由帶負電的微粒組成的帶電微粒說。兩大學派經由實驗證明各自學派的主張,而最後由法國物理學家讓·佩蘭與湯木生證實了陰極射線是帶有電荷的。
實驗主要是由湯木生改良佩蘭教授的實驗,他將聯接到靜電計的電荷接收器安置在真空管的一側,接著利用磁場使射線偏轉,磁場增加至一定程度的時候,接收器接收到的電荷會突然遽增,這說明了這些電荷的產生來自於陰極射線,也因此駁回了乙太說的主張,證實了陰極射線帶有電荷。
電偏轉
[編輯]1897年5月至6月,湯木生研究了光線是否可以被電場偏轉。 以前的實驗者沒有觀察到這一點,但湯木生認為他們的實驗是有缺陷的,因為他們的管子含有太多的氣體。
注釋
[編輯]- ^ 英語人名Thomson在現代人名翻譯中應譯作「湯姆森」,但在指該物理學家時約定俗成譯作「湯木生」(陸譯「湯姆孫」、港譯「湯姆生」)。
參考資料
[編輯]- ^ Rayleigh. Joseph John Thomson. 1856-1940. Obituary Notices of Fellows of the Royal Society. 1941, 3 (10): 586–609. doi:10.1098/rsbm.1941.0024.
- ^ 2.0 2.1 2.2 Joseph John "J. J." Thomson. Science History Institute. June 2016 [20 March 2018]. (原始內容存檔於2021-04-14).
- ^ 3.0 3.1 J.J. Thomson - Biographical. The Nobel Prize in Physics 1906. The Nobel Foundation. [11 February 2015]. (原始內容存檔於2018-07-30).
- ^ 4.0 4.1 Joseph John Thomson. Chemical Heritage Foundation. [18 November 2013]. (原始內容存檔於2015-09-05).
- ^ The Biographical Dictionary of Women in Science: L-Z (頁面存檔備份,存於網際網路檔案館) by By Marilyn Bailey Ogilvie and Joy Dorothy Harvey, Taylor & Francis, p.972
- ^ Thomson, J. J. On the emission of negative corpuscles by the alkali metals. Philosophical Magazine. Series 6. 1905, 10 (59): 584–590. doi:10.1080/14786440509463405.
- ^ Hellemans, Alexander; Bunch, Bryan. The Timetables of Science. Simon & Schuster. 1988: 411. ISBN 0671621300.
- ^ Thomson, J. J. On the Number of Corpuscles in an Atom. Philosophical Magazine. June 1906, 11 (66): 769–781 [4 October 2008]. doi:10.1080/14786440609463496. (原始內容存檔於19 December 2007).
延伸閱讀
[編輯]- Dahl, Per F., "Flash of the Cathode Rays: A History of J.J. Thomson's Electron". Institute of Physics Publishing. June, 1997. ISBN 0-7503-0453-7