芳香性
芳香性(英語:Aromaticity),是一種化學性質,有芳香性的分子中,由不飽和鍵、孤對電子和空軌道組成的共軛系統具有特別的、僅考慮共軛時無法解釋的穩定作用。可以將芳香性看作是環狀離域和環共振的體現。一般認為在這些體系中的電子,可以自由在由原子組成的環形結構上運動(離域),這些環形結構含有單鍵和雙鍵相間,離域的結果是環鍵的鍵級趨於均化,給予體系穩定作用。
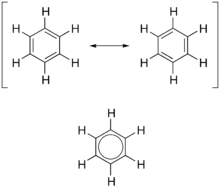
芳香性的理論最初由德國有機化學家奧古斯特·凱庫勒(August Kekulé)發展出來,是以六元的苯分子為原型建立起來。理論中的苯有兩個共振形態,並有單鍵和雙鍵相間,但理論上的兩種苯(環己三烯)衍生物的這類異構體在實際上無法檢測或分離出來,苯事實上是這兩個異構體的「雜化體」,並且具有不考慮電子離域時無法解釋的穩定性。
理論
[編輯]
右上圖中的雙箭頭於化學中代表共振的意思,但不代表該分子會變成那兩個形態,反而是指該分子處於該兩個形態的混合狀態。事實上,那兩個形態都不能代表分子實際的形態,但指出了電子大概的分佈。由此可見,分子真實的形態就是那兩個形態的融合,而它所發出的電磁波波長就是該兩個形態所發出的平均長度。
用組成π鍵的電子密度分佈的位置,來更準確地解釋就是電子分佈在分子的環的上、下。
歷史
[編輯]凱庫勒最初在苯之中發現芳香性這特性,其後於1931年才有人以量子力學來解釋此現象。當年亦證實芳香性之中的π電子的數量必定是4n+2的定律,並肯定芳香族分子的環必定是平面的。而4n+2的概念亦和伍德沃德-霍夫曼規則有所相關。
芳香性化合物的特徵
[編輯]被分類為芳香性的化合物通常有以下的條件:
- 有一些離域電子組成一些π鍵,並且令整個環系統可以當成單與雙鍵的組合;
- 給出離域電子形成π鍵的原子需處於同一個平面;
- 原子需組成一個環;
- 組成π鍵的電子總數需為 4n+2,即不是4的倍數的雙數(休克爾規則);
- 可進行親電芳香取代反應和親核芳香取代反應。
苯就是一個較好的例子,它適合以上所有條件,並且有6個離域電子(即n=1)。有4n+2個π電子的化合物通常都是芳香性的。環丁二烯只有4個離域電子,所以不屬於芳香性化合物。這些只有4n個π電子而又具近似平面結構的環狀化合物稱為反芳香性化合物。
非芳香族的有機物就叫做脂肪族,脂肪族沒有芳香族具有的特殊的共振穩定作用。在受到與平面垂直的外磁場作用時,離域的π電子環電流產生的感應磁場可將整個空間劃分為屏蔽區與去屏蔽區,可在核磁共振結果上顯示出來。
在商業中最重要的芳香化合物就是苯和甲苯,每年產量極高。從石油中得到的苯和甲苯可用來做其他極有用的日用品材料,包括苯乙烯、苯酚、苯胺及尼龍。
芳香性化合物的分類
[編輯]芳香性化合物大致可分為:簡單的芳香化合物、多環芳香化合物和雜環化合物。
雜環化合物
[編輯]雜環化合物之中組成環的原子不僅包括碳,還包括氮、氧或硫等原子,例如五元的吡咯、呋喃和噻吩、六元的吡啶、多環的吲哚、喹啉等。
多環芳香化合物
[編輯]多環芳香化合物中有一類多環芳香烴,其分子由超過一個不包含雜環或取代基的芳香環融合在一起並同時分享兩個碳原子所組成,當中有一些是致癌物質。例子有萘、蒽、菲。
簡單的芳香化合物
[編輯]芳香烴有大量的有機化合物的結構當中都包含簡單的芳香環,例如DNA(包含嘌呤、嘧啶等)、三硝基甲苯(含苯環)、乙醯水楊酸(含苯環)和對乙醯氨基酚(含苯環)等。



