揮發性
此條目可參照英語維基百科相應條目來擴充。 (2021年8月8日) |

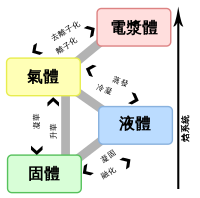
揮發性,在化學、物理和熱力學的領域中,是指物質汽化的容易程度。在一特定的溫度與壓力下,高揮發性的物質更傾向於以氣體形式存在,而低揮發性的物質,更傾向於以液體或是固體形式存在。揮發性也可以用來描述氣體凝結成液體或固體的傾向性,低揮發性物質比高揮發性物質更容易凝結。[1] 物質間的揮發性差異,可由觀察其在空氣中蒸發或昇華的快慢來得知,高揮發性的物質,例如異丙醇,會快速的蒸發,而低揮發性的植物油則會保持在液態。[2]一般來說,固體比液體揮發性低,但也有例外,如乾冰或碘可以在標準狀況下昇華成氣態。
簡介
[編輯]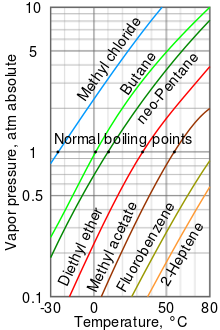
揮發性本身沒有定量的數值定義,但通常使用蒸氣壓或沸點(液體)來描述。高蒸氣壓指高揮發性,而高沸點指低揮發性。蒸氣壓和沸點通常以表格和圖表的形式呈現,可用於比較不同的物質,而這些數據通常是通過在一定溫度和壓力範圍內的實驗得出的。
蒸氣壓
[編輯]蒸氣壓用來量化物質在特定溫度下形成蒸氣的難易程度。當一個物質被封閉在真空密封容器內時,會迅速用蒸汽填充該空間,在系統達到平衡且不再形成蒸汽後,可以測量該蒸汽壓力。增加溫度會增加形成的蒸汽量,從而增加蒸汽壓。在混合氣體中,每種物質都會貢獻混合物的總蒸氣壓,而其中揮發性更強的物質會產生更大的貢獻。
沸點
[編輯]沸點是當液體的蒸氣壓等於周圍壓力時的溫度,此刻,液體迅速蒸發(沸騰)。這數值與蒸氣壓相關,但取決於環境壓力。一般來說,沸點是指物質在一大氣壓下的沸點,但在其他壓力下也可以被測量與紀錄。[3]
影響因素
[編輯]分子間作用力
[編輯]影響物質揮發性的一個重要因素是其分子間作用力。分子間的吸引力是將物質結合在一起的原因,具有更強分子間作用力的物質(例如大多數固體)通常不易揮發。乙醇和二甲醚這兩種具有相同化學式(C2H6O)的化學物質,由於它們在液相中分子間作用力不同,而具有不同的揮發性。乙醇分子能夠形成氫鍵,而二甲醚分子不能,這導致乙醇分子間的整體吸引力更強,而有較低的揮發性。[4]
分子量
[編輯]一般來說,揮發性會隨著分子量的增加而降低,因為較大的分子可以參與更多的分子間鍵結,儘管結構和極性等其他因素也會起重要作用。通過比較具有相似結構的化學物質,可以部份獨立出分子量的影響。例如,隨著碳鏈中碳數的增加,直鏈烷烴的揮發性會降低。
應用
[編輯]蒸餾
[編輯]
對揮發性的了解可以用來分離混合物。當凝相的混合物包含多種不同揮發性的物質時,可以控制其溫度和壓力,以使更易揮發的成分變成蒸氣,而不易揮發的物質則保留在液相或固相中。形成的蒸氣可以被丟棄或冷凝到另外的容器中,如果蒸氣是被收集,這過程稱為蒸餾。
石油精煉過程利用一種稱為分餾的技術,能夠在一個步驟中分離出幾種揮發性不同的化學物質。原油是由各種有用的物質組成,而它們需要被分離才能有效使用。原油流入蒸餾塔並被加熱,使丁烷和煤油等更易揮發的成分蒸發。這些蒸氣向上移動並最終與較冷的表面接觸,從而使它們冷凝並被收集。最易揮發的化學物質在塔頂冷凝,而最不易蒸發的化學物質在最低部分冷凝。
傳統上,精製酒精會利用到水和乙醇之間的揮發性差異。為了增加產品中乙醇的濃度,酒精製造商會將初始酒精混合物加熱到大部分乙醇蒸發而大部分水保持液態的溫度,然後收集乙醇蒸氣並在單獨的容器中冷凝,從而得到更濃縮的產品。
香水
[編輯]在製作香水時,揮發性是一個重要的考慮因素,當芳香蒸氣與鼻子中的受體接觸時,人體會檢測到氣味。在香水被塗抹後,其中較易迅速蒸發的成分會在油蒸發之前的短時間內產生芳香的蒸汽。而緩慢蒸發的成分可以在皮膚上停留數週甚至數月,但可能不會產生足夠的蒸汽來產生強烈的香氣。為了避免這些問題,香水設計師會仔細考慮香水中精油和其他成分的揮發性,並通過改變高揮發性和非揮發性成分的量來實現適當的蒸發速率。
參見
[編輯]參考文獻
[編輯]- ^ Felder, Richard. Elementary Principles of Chemical Processes. John Wiley & Sons. 2015: 279–281. ISBN 978-1-119-17764-7.
- ^ Koretsky, Milo D. Engineering and Chemical Thermodynamics. John Wiley & Sons. 2013: 639–641. ISBN 978-0-470-25961-0.
- ^ Zumdahl, Steven S. Chemistry. Houghton Mifflin. 2007: 460-466. ISBN 978-0-618-52845-5.
- ^ Atkins, Peter. Chemical Principle. W. H. Freeman. 2012. ISBN 978-1-4292-8897-2.