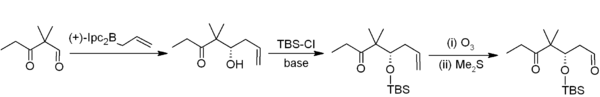有機硼化合物
有機硼或有機硼化合物是一類硼烷BH3的有機衍生物,如:三烷基硼烷。有機硼化學或有機硼烷化學是研究這類化合物的化學。[1][2] 在有機化學中,有機硼化合物因其多種變化而被廣泛應用,其中如常用的還原反應:硼氫化反應。
理化性質
[編輯]碳-硼鍵屬低極性化學鍵(其元素電負性差別:碳2.55;硼2.04),因此烷基硼化合物雖大多易於氧化但性質較穩定。乙烯基和芳基連於硼原子上,會提供電子給硼原子使得其具有更小的電負性,並讓碳-硼鍵具有一定的雙鍵特性。有機硼烷類似於其母體乙硼烷的性質,屬於有機化學中較強的親電試劑,這是由於硼原子無法得到八隅體的的全部電子。不同於乙硼烷的是,有機硼烷化合物不形成二聚體。
其他有趣的硼烷,例如碳硼烷化合物,屬於碳、硼與硼代苯的原子簇化合物,其硼和苯為等當量。環狀化合物硼咯,是一種吡咯的結構類似物 ,至今無法分離,但其取代衍生物已經被發現。
有機硼烷化合物的氧原子可被取代,得到二烴基硼酸酯R2BOR、單烴基硼酸酯RB(OR)2或硼酸酯B(OR)3,如:三甲基硼酸酯。在有機金屬化學中,帶有硼-金屬鍵的化合物統稱為:硼基(M–BR2)或亞硼基(M–B(R)–M)。
合成
[編輯]從格氏反應合成
[編輯]簡單的有機硼烷,如:三乙基硼烷或三(全氟苯基)硼烷可通過三氟化硼(通常為乙醚的絡合物)來製備,或通過乙基或全氟苯基硼烷與格氏試劑反應製備。
從烯烴合成
[編輯]硼烷與烯烴可迅速發生反應,稱為:硼氫化反應。這個概念由赫伯特·布朗在普渡大學發現,並由此獲得了諾貝爾獎(與發現維蒂希反應的化學家格奧爾格·維蒂希共同獲得)。乙硼烷通常以二聚體存在,而BH3單體可與鹼性溶劑,如四氫呋喃形成1:1的絡合物。在簡單的HX(X = Cl,Br,I等)參與的親電加成反應中均符合馬氏規則,即:最小電負性的原子(通常為氫原子),加成至雙鍵上最少取代基的一側,這決定了區域選擇性。硼對於雙鍵的親電加成同樣如此,由於硼元素的電負性較氫元素更弱,氫原子總是加成於取代最多的碳原子上。烯烴上形成的正電荷在取代基最多的碳原子上,部分負電荷的氫原子與之加成,留下的硼原子加成於取代基更少的碳原子上。上述的這種加成方式,稱為「反馬氏規則」,當硼原子被羥基取代後,水對於雙鍵的加成就是符合反馬氏規則。
當硼化合物帶有大位阻取代基時,其化學性質很特別。如一種有機硼化合物常用於有機合成:9-BBN。該化合物可通過環辛二烯與乙硼烷反應製備。[3] 在順式硼氫化過程中會發生立體專一性,即在烯烴的同一面進行加成反應。在該協同反應中,過渡態表示為一種被由碳原子、氫原子與硼原子組成的正方形。在此正方形中,在兩個雙鍵、p-軌道和硼原子的空軌道的之間具有最大電子云重疊。
反應
[編輯]硼氫化氧化
[編輯]在有機合成中,硼氫化反應常用於通過引入硼基團而繼續轉化為其他官能團。硼氫化-氧化反應通過先與硼烷加成,後使用過氧化氫氧化提供了一種合成醇的方法。該反應過程中,若將氧化劑替換成氧化鉻,將使得羥基繼續氧化成羰基化合物。
重排反應
[編輯]有機硼化合物可參與引入新的碳-碳鍵的化學反應。一氧化碳被發現易與三烷基硼烷發生反應。當負電性的硼原子上有烷基取代基時可發生1,2-重排反應,該烷基可重排至臨近的親電性的羰基碳原子上。而羰基可進一步還原為羥基。
烯丙基硼烷化
[編輯]烯丙位不對稱硼化展示了有機硼化合物在碳-碳鍵形成反應中的另一個應用實例。[4] 在Nicolaou合成了埃博黴素[5]的例子中,使用了手性α-蒎烯衍生出的不對稱烯丙基硼化反應,該反應用於連接TBS保護基(叔丁基二甲基硅烷)並繼而發生臭氧分解反應。
金屬轉移反應
[編輯]有機硼化合物還可與有機鈀化合物發生金屬轉移反應。該反應類型在鈴木反應中被廣泛應用。
參與氧化還原反應
[編輯]混合硼烷,如9-BBN和三仲丁基硼氫化鋰(L-selectride)屬於一類還原劑。例如羰基還原反應中的不對稱催化劑就是CBS催化劑。該催化劑屬有機硼催化劑,用於反應中與羰基氧原子配位。
三苯基硼或三(α-萘基)硼和鈉汞齊反應,可以得到Na[BPh3]或Na2[BNp3](Np=萘基)。[6][7]
硼酸酯
[編輯]三烷基硼烷,BR3可氧化為相應的硼酸的形式B(OR)3。鑑定化合物中具有的C-B鍵的數量,可通過R3B被三甲胺氧化物(Me3NO)氧化成B(OR)3後,滴定形成的三甲胺的量來測算。
硼酸RB(OH)2與氟氫化鉀(K[HF2])反應,形成三氟硼酸鹽 K[RBF3] [8],該物質是親核性烷基或芳基二氟硼酸鹽ArBF2 的前體[9],該化合物鹽的形式比起硼酸本身更穩定,因此常用於特定醛的烷基化反應。
硼基鋰
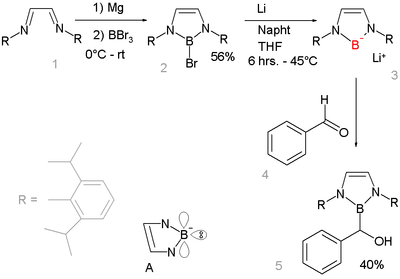
[編輯]親核性的硼基負離子化合物長久以來未受重視,從2006年以來研究發現了一種硼基鋰化合物,可作為很強的親核試劑[11][12]:
這個發現非常重要,因為其他的第二周期元素組成的鋰化合物較常見,如:氟化鋰,氫氧化鋰,氨基鋰以及其他的有機鋰化合物。鹼和硼氫化合物 R2B反應不會導致去質子化形成硼基負離子R2B-,而是形成硼基負離子R2B-H(base)+,這是因為反應過程中不能形成完整的八隅體。[13]
亞烷基硼
[編輯]亞烷基硼具有RB=CRR的形態:一個硼原子與一個碳原子組成雙鍵,是一種少見的化合物類型,如硼苯。其母體化合物為HB=CH2,可在低溫下檢測到。還有一種很穩定的衍生物為:CH3B=C(SiMe3)2,但非常容易發生環二聚反應。[14]
二硼烯烴
[編輯]帶有硼-硼雙鍵的化合物相當罕見,直到2007年第一個中性的二硼烯烴化合物(RHB=BHR)才被發現[15][16][17] 這種化合物的每個硼原子都連接了一個質子,且每個硼原子都和氮雜環卡賓[18]配位。
注釋
[編輯]參見
[編輯]- 在元素周期表中碳元素與其他元素組成的化合物
參考文獻
[編輯]- ^ The Roles of Boron and Silicon, Susan E. Thomas; Oxford Chemistry Primers No.1; 1991: Very good general book covering all the important reactions of boron and organoboranes in organic chemistry.
- ^ Organometallics Christoph Elschenbroich 3rd Ed. 2006 ISBN 3-527-29390-6 – Wiley-VCH, Weinheim
- ^ Advanced Organic Chemistry, F.A. carey, R.J. Sundberg ISBN 0-306-41088-5
- ^ Lachance, H.; Hall, D. Org. React. 2008, 73, 1. (doi: 10.1002/0471264180.or073.01)
- ^ Nicolaou, K.C.; Sarabia, F.; Ninkovic, S.; Finlay, M.R.V.; Boddy, C.N.C. Probing The Ring Size Of Epothilones: Total Synthesis Of 14-, 15-, 17-, And 18 Epothilones A. Angewandte Chemie. International edition in English. 1998, 37 (1–2): 81–84 [2008-03-02]. (原始內容存檔於2012-03-14).
- ^ Bent, Henry E.; Dorfman, Maurice. PENTAVALENT BORON. Journal of the American Chemical Society (American Chemical Society (ACS)). 1932, 54 (5): 2132–2133. ISSN 0002-7863. doi:10.1021/ja01344a511.
- ^ Bent, Henry E.; Dorfman, Maurice. The Conductance of Non-aqueous Solutions. I. Sodium Triphenylboron and Disodium Tri-α-naphthylboron in Diethyl Ether. Journal of the American Chemical Society (American Chemical Society (ACS)). 1935, 57 (10): 1924–1927. ISSN 0002-7863. doi:10.1021/ja01313a051.
- ^ Conversion of Arylboronic Acids into Potassium Aryltrifluoroborates: Convenient Precursors of Arylboron Difluoride Lewis Acids E. Vedejs, R. W. Chapman, S. C. Fields, S. Lin, M. R. Schrimpf J. Org. Chem. 1995; 60(10); 3020–3027. doi:10.1021/jo00115a016
- ^ Organotrifluoroborates and Monocoordinated Palladium Complexes as Catalysts—A Perfect Combination for Suzuki–Miyaura Coupling Gary A. Molander and Belgin Canturk Angew. Chem. Int. Ed. 2009, 48, 9240 – 9261doi:10.1002/anie.200904306
- ^ Organoboron compounds as mild nucleophiles in Lewis acid- and transition metal-catalyzed C–C bond-forming reactions Robert A. Batey, Tan D. Quach, Ming Shen, Avinash N. Thadani, David V. Smil, Sze-Wan Li, and D. Bruce MacKay Pure Appl. Chem., Vol. 74, No. 1, pp. 43–55, 2002. http://www.iupac.org/publications/pac/2002/pdf/7401x0043.pdf (頁面存檔備份,存於網際網路檔案館)
- ^ Boryllithium: Isolation, Characterization, and Reactivity as a Boryl Anion Yasutomo Segawa, Makoto Yamashita, Kyoko Nozaki Science 6 October 2006: Vol. 314. no. 5796, pp. 113 – 115 doi:10.1126/science.1131914
- ^ Boron Attacks Electropositive element pressed into action as nucleophilic boryllithium Bethany Halford Chemical & Engineering News October 9, 2006 Volume 84, Number 41 p. 11 Link (頁面存檔備份,存於網際網路檔案館)
- ^ Boronic Acids: Preparation, Applications in Organic Synthesis and Medicine. Dennis G. Hall ISBN 3-527-30991-8
- ^ Reactions at the Boron-Carbon Double Bond of Methyl(methylidene)boranes Peter Paetzold, Ulli Englert, Rudolf Finger, Thomas Schmitz, Alexander Tapper, and Ralf Ziembinski Z. Anorg. Allg. Chem. 2004, 630, 508–518 doi:10.1002/zaac.200300396
- ^ A Stable Neutral Diborene Containing a BdB Double Bond Yuzhong Wang, Brandon Quillian, Pingrong Wei, Chaitanya S. Wannere, Yaoming Xie, R. Bruce King, Henry F. Schaefer, III, Paul v. R. Schleyer, and Gregory H. Robinson doi:10.1021/ja075932i
- ^ Neutral Diborene Is A First Ron Dagani Chemical & Engineering News October 1, 2007 Volume 85, Number 40 p. 10 [1] (頁面存檔備份,存於網際網路檔案館)
- ^ 反應的硼前體為三溴化硼,還原劑為KC8,它可以從乙醚溶劑當中提取質子。
- ^ 也譯作穩定卡賓