液相色譜法-質譜聯用
 Ion trap LCMS system with ESI interface | |
| 英文缩写 | LCMS |
|---|---|
| 分类 | 層析法 質譜法 |
| 分析对象 | 有機分子 生物分子 |
| 生产厂家 | 安捷倫科技 Bruker MDS 珀金埃尔默 岛津制作所 赛默飞世尔科技 Varian, Inc. Waters Corporation |
| 其它技术 | |
| 其它技术 | 氣相色譜法-質譜聯用 |
液相層析法-質譜聯用(英語:Liquid chromatography–mass spectrometry,英文缩写LC-MS)是一種將液相層析(Liquid chromatography,簡稱LC)的物理分離能力和質譜(mass spectrometry,簡稱MS)的質量分析能力結合起來的分析化學技術。LC-MS是一項具有非常高的敏感度和選擇性的非常強而有力的分析技術,它使用於很多的領域。一般說來,它的使用方向是在多種其他化合物存在的複合混合物中,測出各種組分並有可能確定其詳細結構。 LC-MS在尿液中藥物篩選分析中的局限性在於它常常不能區分特定的代謝產物,特別是對於氫可酮及其代謝物尤為明顯。LC-MS尿液分析測試僅測定特定類別的藥物,對於有些藥物及其代謝物的測定需要用氣相層析法-質譜聯用(Gas chromatography-mass spectrometry,簡稱 GC-MS)
液相層析法
[编辑]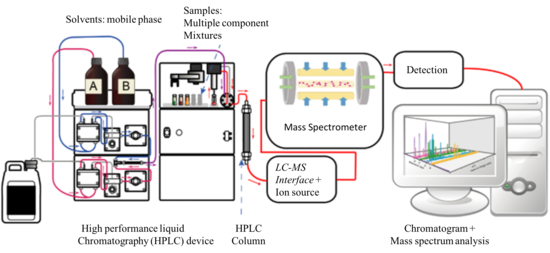
規模
[编辑]傳統的高效液相色譜方法與用於LC-MS中的液相色譜方法的主要不同是後者的規模要小得多。色譜的規模與色譜柱的內徑相關以及流速相關。其規模與柱內徑的平方成正比。在一個相當長的時間裡,LC-MS的工作色譜柱內徑為1 mm,而與之對應HPLC的色譜柱內徑為4.6 mm)。最近,300 µm 和甚至 75 µm的毛細管柱已經成為更為普遍的選擇。在這些直徑的柱子的下端流速接近100 nL/min,並且一般被用於納米噴霧源。[1]
分流
[编辑]當使用標準細徑(4.6 mm)柱時,所采用的分流比是~10:1。這樣做的益處是可以允許串聯使用其他檢測技術,如MS和UV。然而,分流到UV會降低光電檢測器的敏感度。另一方面,質譜在流速不大于200 μL/min時可對靈敏度有所改善。
質譜方法
[编辑]質譜分析器
[编辑]有許多不同的質譜分析器可以用于LC/MS。單個四極桿分析器(Single Quadrupole analyzer)、三重四極桿分析器(Triple Quadrupole analyzer)、離子阱分析器(Ion Trap analyzer)、飛行時間質譜分析器(Time-of-flight mass spectrometry)以及四極桿飛行時間兩種質譜分析器的結合(Q-TOF)。
接口
[编辑]在連續流動的液體的液相技術與在真空中進行的氣相技術之間進行銜接長期以來都是困擾著氣質聯用技術的一項大的困難。電噴離子化出口的的出現克服了這一困難。最常用的銜接界面是電噴離子源或其變種納米離子源;然而,人們也還使用大氣壓化學離子化界面。[2]人們也使用各種沉積和干燥技術,比如,使用移動帶;然而,最普通的沉積干燥技術是基質輔助雷射脫附/游離(Matrix-assisted laser desorption/ionization,簡稱MALDI)[3][4]目前,一種仍在開發中的新方法叫做直接電離子化LC-MS 接口(Direct-EI LC-MS interface),是將納米級色譜和裝備電離子化的質譜結合的產物。
應用
[编辑]藥代動力學
[编辑]LC-MS非常普遍地用于藥物的藥代動力學的研究,并且是生物分析中最常使用的技術。這些研究給出關于藥物在肝臟血流,和人體其他器官中清除的速率。這類研究中使用MS的原因是MS與UV相比較有更高的敏感度和超乎一般的特異性(只要被分析物可以被離子化),和較短的分析時間。
MS的主要優點是它使用串聯質譜(MS-MS)。可以給檢測器編程,讓它選擇某種離子,將其斷裂成碎片。這個過程是從根本上講是選擇技術,但是事實上要復雜得多。被測量的量是操作者所選擇的分子碎片的總合。只要沒有干擾和離子抑制作用,色譜分離會進行的特別快,目前用MS-MS檢測器的分析時間是不到1分鐘,而使用UV檢測器要超過10分鐘。[5][6][7]
LC-MS也用于研究蛋白質組學。在蛋白質組學中,人們遇到的也是要在複合混合物體系中檢測出某些組分并用某種方法確定其詳細結構。用于蛋白質組的自下而上(bottom-up proteomics)的LC-MS方法一般涉及蛋白酶解消化和變性(通常,選用胰蛋白酶進行酶解消化,用尿素將三級結構變性,用碘乙酰胺給半胱氨酸“戴帽”,最后,用LC-MS肽質譜指紋區(peptide mass fingerprinting)或LC-MS/MS串聯質譜去推導各個多肽的序列。[8] )LC-MS/MS通常用于復雜試樣的蛋白質組分析。對于復雜試樣即使用高分辨率的質譜儀多肽的質量也可能發生重疊。像人的血清那樣的復雜生物體液試樣只要首先使用SDS-PAGE凝膠電泳或HPLC-SCX進行分離,都可以在現代的LC-MS/MS系統中操作并且可以定出1000種以上蛋白分子的結構。然而,只有在通過SDS-PAGE凝膠或HPLC-SCX分離樣品之後,這種高水平的蛋白質鑑定才是可能的。
LC-MS也用於分析天然產物和分析植物的次级代谢产物[9]。在這方面,基於質譜的系統有助於從復雜的生物植物樣本中獲取更多關於化合物範圍廣泛的信息。
藥物開發
[编辑]LC-MS也頻繁地用于藥物開發的許多不同的階段,包括,做肽圖、做醣蛋白圖、天然產物的去重復化、生物親和性篩選。體內藥物篩選、代謝穩定性篩選、代謝物結構確定、雜質確定、降解產物的結構確定、定量生物分析和質量控制。[10]
參見
[编辑]- 氣相色譜法-質譜聯用 (GC-MS)
- Capillary electrophoresis–mass spectrometry
- Ion-mobility spectrometry–mass spectrometry
參考資料
[编辑]- ^ Capillary liquid chromatography/mass spectrometry, Kenneth B. Tomer, M. Arthur Moseley, Leesa J. Deterding, Carol E. Parker, Mass Spectrometry Reviews, Vol 13, 1994, pp 431-457
- ^ Combined liquid chromatography mass spectrometry. Part III. Applications of thermospray, Patrick Arpino, Mass Spectrometry Reviews, Vol 11, 1992 pp 3-40
- ^ Combined liquid chromatography mass spectrometry. Part I. Coupling by means of a moving belt interface, Patrick Arpino, Mass Spectrometry Reviews, Vol 8, 1989 pp 35-55
- ^ Coupling matrix-assisted laser desorption/ionization to liquid separations, Kermit K. Murray, Mass Spectrometry Reviews, Vol 16, pp 283-299[永久失效連結]
- ^ Increasing Speed and Throughput When Using HPLC-MS/MS Systems for Drug Metabolism and Pharmacokinetic Screening, Y. Hsieh and W.A. Korfmacher, Current Drug Metabolism Volume 7, Number 5, 2006, Pp. 479-489
- ^ Covey TR, Lee ED, Henion JD. 1986. High-speed liquid chromatography/tandem mass spectrometry for the determination of drugs in biological samples. Anal Chem 58:2453-2460.
- ^ Thermospray liquid chromatography/mass spectrometry determination of drugs and their metabolites in biological fluids. Covey TR et al. Anal Chem. 1985 Feb;57(2):474-81
- ^ Wysocki VH, Resing KA, Zhang Q, Cheng G. Mass spectrometry of peptides and proteins. Methods. March 2005, 35 (3): 211–22. PMID 15722218. doi:10.1016/j.ymeth.2004.08.013.
- ^ Stobiecki, M.; Skirycz, A.; Kerhoas, L.; Kachlicki, P.; Muth, D.; Einhorn, J.; Mueller-Roeber, B. Profiling of phenolic glycosidic conjugates in leaves of Arabidopsis thaliana using LC/MS. Metabolomics. 2006, 2 (4): 197–219. doi:10.1007/s11306-006-0031-5.
- ^ LC/MS applications in drug development, Mass Spectrometry Reviews, Mike S. Lee, Edward H. Kerns, Vol 18, 1999, pp 187-279[永久失效連結]
有關書目
[编辑]- Thurman, E. M.; Ferrer, Imma. Liquid chromatography/mass spectrometry, MS/MS and time of flight MS: analysis of emerging contaminants. Columbus, OH: American Chemical Society. 2003. ISBN 0-8412-3825-1.
- Ferrer, Imma; Thurman, E. M. Liquid chromatography-Time of Flight Mass Spectrometry: Principles, Tools and Applications for Accurate Mass Analysis. New York, NJ: Wiley. 2009. ISBN 978-0-470-13797-0.
- Ardrey, R. E.; Ardrey, Robert. Liquid chromatography-mass spectrometry: an introduction. London: J. Wiley. 2003. ISBN 0-471-49801-7.
- McMaster, Marvin C. LC/MS: a practical user's guide. New York: John Wiley. 2005. ISBN 0-471-65531-7.
- Wilfried M.A. Niessen, Wilfried M. Niessen. Liquid Chromatography-Mass Spectrometry, Third Edition (Chromatographic Science). Boca Raton: CRC. 2006. ISBN 0-8247-4082-3.
- Yergey, Alfred L. Liquid chromatography/mass spectrometry: techniques and applications. New York: Plenum Press. 1990. ISBN 0-306-43186-6.
